Notícia
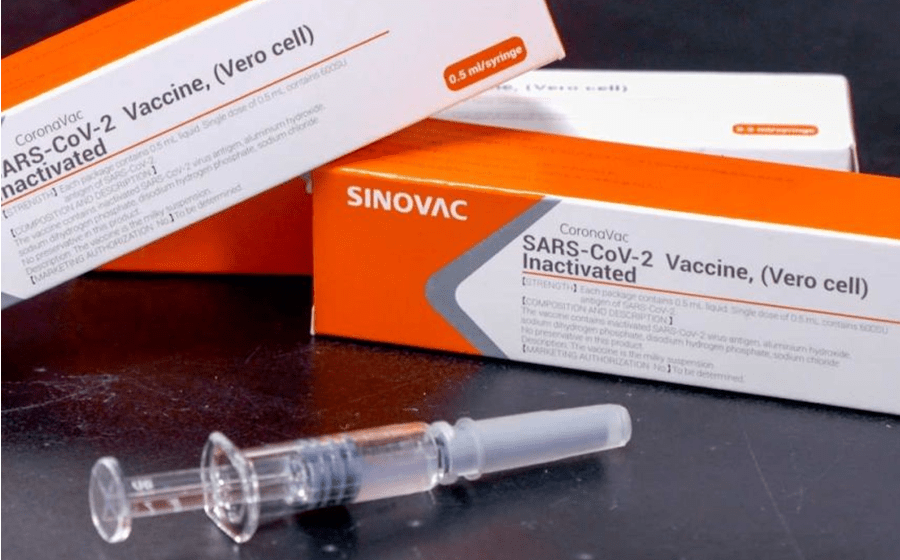
Regulador brasileiro autoriza reinício dos testes da vacina chinesa CoronaVac
Depois do Brasil ter suspendido na noite de segunda-feira a realização dos testes da vacina CoronaVac, devido à morte de um participante, a Anvisa retomou esta quarta-feira a realização dos mesmos.
A Agência Nacional de Vigilância Sanitária (Anvisa), reguladora brasileira do setor da saúde, autorizou o reinício dos ensaios realizados com a vacina chinesa contra a Covid-19, que tinham sido suspensos na noite de segunda-feira (9 de novembro) devido a um "evento adverso grave".
Ao longo do dia 9 de novembro, todas as entidades envolvidas na situação deram a conhecer os seus pareceres e dois dias depois a Anvisa, após analisar os riscos e benefícios associados à toma da vacina, volta a assegurar a realização da experiência, segundo a Folha de São Paulo.
De acordo com as declarações do diretor do instituto Butantan, Dimas Covas, à Folha de São Paulo, o falecimento não está relacionado com a administração da vacina. Sendo que o que levou à morte do voluntário, um químico de 32 anos, ou foi o suicídio, ou uma overdose, segundo apuraram os especialistas.
Mal tomou conhecimento do sucedido, a Anvisa determinou a interrupção do estudo clínico com o intuito de apurar a verdade e perceber os riscos e benefícios associados à vacina chinesa, realizada pela empresa Sinovac em parceira com o instituto Butantan. Após analisar a situação, a Anvisa decidiu o veredito da vacina, aprovando a retoma dos testes. Contudo, salienta que irá acompanhar com mais atenção esta testagem e continuar a estudar a possível relação entre a morte do voluntário e a vacina.
De acordo com a médica epidemiologista Denise Garrett, "na interrupção dos testes da CoronaVac, a Anvisa, o Butantan e Bolsonaro erraram". Contudo, se algo mais sério acontece a algum voluntário, como sequelas, incapacidade ou morte, os cientistas necessitam de alertar as agências que acompanham e aprovam todo o processo, neste caso específico a Anvisa.
Para o diretor da Anvisa, António Barra Torres, os testes foram interrompidos pelo facto de a agência ter recebido informações incompletas por parte do Butantan acerca do caso. Todavia, a Anvisa salientou à Folha de São Paulo que, tendo em conta a informação que tinha necessitava de analisar a situação e apurar a veracidade da problemática.
A Anvisa disse ainda, num comunicado, que "a suspensão de um produto não significa necessariamente que não tenha qualidade, segurança, ou eficácia" e reforçou que ocorrem diversas suspensões em estudos clínicos só para garantir que estes são seguros para os voluntários.
A vacina chinesa encontra-se na terceira fase de testes desde dia 21 de julho no Brasil, Turquia e Indonésia.